作者:雪球用户先信资本
和誉当前拥有一个已基本成药的10亿美元分子「Pimicotinib」,一个高确定性、具备前线拓展空间的25亿美元分子「ABSK011」,分别将在26H2、27-28年实现商业化并贡献现金流。这两款药物即可支撑起公司百亿港元市值(「ABSK011」BD的前提下)。
此外,和誉还拥有两个销售峰值超过50亿美元的高潜分子「ABSK061」、「ABSK043」,将在25年底-26年迎来催化。这两款药物将成为公司走向200亿-300亿港元市值的台阶。
一、回购+增持诚意满满
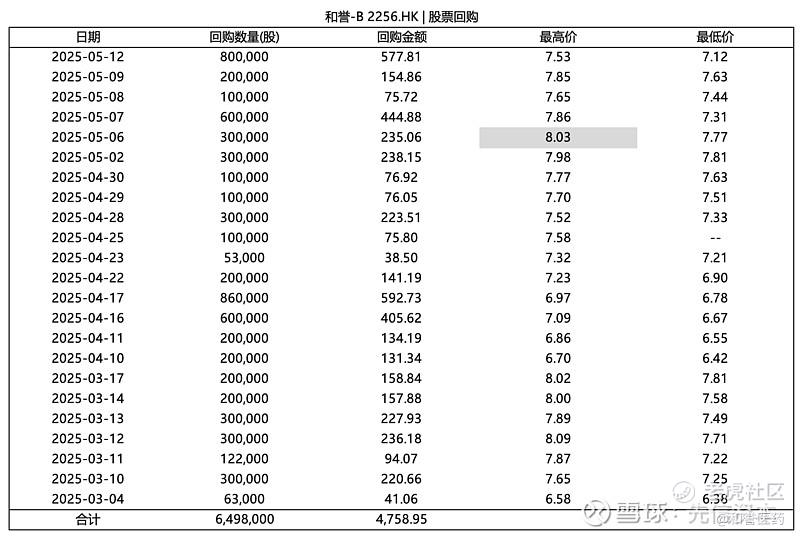
自新一轮回购计划发布以来(25.03-25.05),和誉共斥资4758.95万元回购了649.80万股,最高回购价格8.03港元。在此期间,实控人徐博共增持11.5万股,其中5月6日增持均价7.957港元。
回购、增持双线并行,彰显管理层对于基本面的信心,对于未来现金流的信心。
二、管线看点十足
1. Pimicotinib(CSF-1R)
1)TGCT方面,「Pimicotinib」对比竞品「Vimseltinib」、「Pexidartinib」表现出全球最佳第25周ORR数据(54% vs 40% vs 38%),展现BIC潜力。
2)cGvHD方面,20mg QD亚组患者中已初步观察到64%的ORR(ASH2024发布)。截至数据发布日,大多数患者尚未完成6个月的治疗周期,随着治疗时间的延长,最终数据还会有很大程度的提升。
3)「Pimicotinib」在帕金森、阿尔茨海默等领域亦有应用潜力,后续Merck若开发这些适应症,将会给和誉带来额外的前期付款和里程碑。
4)TGCT全球销售峰值为5-6亿美元(推算过程见笔者往期文章),销售分成比例15%,仅单适应症远期每年就能够为和誉带来0.75-0.90亿美元的收入。
2. ABSK011(FGFR4)
1)2L HCC方面,I期临床完整数据已经发布,在「ABSK011」220mg BID组中,ICIs和mTKIs经治患者的ORR达到44.8%,最长DoR达到16.4m,mDoR达到7.4m,mPFS达到5.5m。
2)1L HCC方面,II期临床初步结果已经发布,在「ABSK011」220mg BID联用阿替丽珠单抗队列中,整体患者ORR高达50%、mPFS为8.3m(未成熟),且对于ICI经治患者疗效同样显著。「ABSK011」+阿替丽珠二联方案有望成为首个获批的1L HCC标准治疗方案。
3)「ABSK011」BD的时间节点有两种可能:1)1L HCC II期临床完整结果发布后;2)2L HCC注册临床入组完成。潜在BD合同可能为:2-2.5亿美元(首付款)+20-25美元(里程碑)+销售分成。
4)销售峰值看,预计「ABSK011」前线+后线销售峰值超25亿美元(推算过程见笔者往期文章)。
3. ABSK061(FGFR2/3)
1)癌症方面,非头对头横向对比,「ABSK061」在早期小样本中的ORR、DCR数据分别为37.5%、50%,接近已上市药物「厄达替尼」、「佩米替尼」,且初步展现出优秀的安全性(未报告高磷血症),若后续扩展数据能够维持,大概率将成为BIC候选。
2)ACH领域,「ABSK061」高选择性靶向FGFR2、FGFR3,既能规避靶向FGFR1带来的高磷血症风险,又能够通过双靶实现比单靶药物更好的年化生长速度。「ABSK061」很可能在临床上能够读出优于「Vosoritide」(FGFR3)且不逊于「Infigratinib」(FGFR1/2/3)的疗效数据,以及接近「Vosoritide」且优于「Infigratinib」的安全性数据,具有BIC潜力。
3)「ABSK061」已经得到「Vosoritide」开发方BioMarin、「Infigratinib」开发方Bridgebio的关注,并已经开始与BioMarin开展一些技术层面上的合作。合理推断,在早期临床数据读出后,「ABSK061」即将迎来BD机会。
4)分别参考海外券商对于「厄达替尼」、「佩米替尼」以及「Vosoritide」全球销售峰值的测算,预计「ABSK061」全球销售峰值有望超过50亿美元(癌症30亿美元+ACH 20亿美元)。
4. ABSK043(Oral PD-L1)
1)「ABSK043」目前处于临床II期,在同class中进度最快。竞品INCB-86550/INCB-99280/INCB-99318(Incyte)研发中断,MAX-10181(MaxNovel)、Amgen(CCX-559)、BPI-371153(贝达)仍处于临床前阶段。
2)相比K药等主流静脉注射PD-(L)1药物,「ABSK043」疗效相当但安全性更优。I期临床中,PD-L1 TPS高表达组、EGFR突变组和KRAS突变组的ORR率分别为41.7%、33.3%、66.7%,与K药相当。安全性数据方面,大多数异常为检查异常(皮疹导致停药),TRAEs≥3级发生率8.8%(K药10%-30%),未观察到ILD(K药3%-5%)。
3)MNC目前还在卷皮下剂型,MSD的K药、BMS的O药均在进行静脉注射→皮下注射的剂型升级。相比皮下剂型,「ABSK043」小分子结构口服给药更加便利,同时无免疫原性,具有更优的副作用管理,有望得到MNC的青睐。
4)销售峰值看,「ABSK-043」销售峰值超50亿美元(推算过程见笔者往期文章)。
三、催化众多,值得期待
1. 「Pimicotinib」计划分别于25年中、25H2、26Q1递交中、美、欧地区NDA,预计中、美26H2获批,欧洲27H1获批。成功获批后,一方面,和誉将获得Merck支付的NDA里程碑付款,推测为每个地区1000万美元,共3000万美元,增厚现金储备;另一方面,和誉将最快在26H2取得销售分成收入,产生正向现金流入(仅TGCT单适应症远期每年0.75-0.90亿美元)。总体估算下来,26年「Pimicotinib」将为和誉贡献4000-5000万美元利润。
2. 「ABSK011」联合阿替丽珠的II期临床完整结果将于ESMO GI 2025(25.07)发布,该数据将支撑「ABSK011」向前线拓展,并取得大额的BD合约,带来2-2.5亿美元+首付款收入;「ABSK011」单药治疗2L HCC的关键注册临床将于25年中启动,计划26年完成患者入组,27-28年实现商业化,开始贡献销售收入。
3. 「ABSK043」预计将在25Q4读出初步安全性数据。MSD、BMS在静脉注射PD-(L)1领域的竞争已逐渐白热化,综合优势更强的「ABSK043」势必会在临床数据读出后得到big pharma的关注,取得BD的机会。


精彩评论