近日,NMPA正式批准卡匹色替(Truqap)联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发且伴有一种或多种PIK3CA/AKT1/PTEN改变的HR+/HER2-乳腺癌成人患者,Truqap成为国内首个获批的AKT抑制剂。
过去,AKT抑制剂Truqap在刚上市之初,该分子并不被市场看好,以“积极的预测”著称Evaluate Pharma,其分析师预测Truqap的远期峰值销售额约为6.9亿美元。
大超预期的是,得益于其在乳腺癌、前列腺癌两大适应症领域的快速推进,不仅其在上市首年2024年就取得了4.3亿美元的销售,并且美银美林更是给出了远期高达38亿美元的销售峰值预测。
Truqap的持续超预期,不仅在提醒着市场小分子的“宝刀未老”,并且让市场重新审视PI3K/AKT/mTOR通路治疗机制的内在价值。
01
通路潜力与Truqap过关斩将
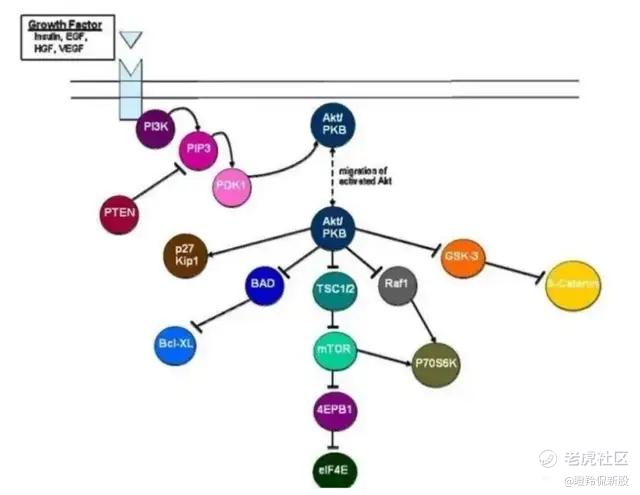
PI3K/AKT/mTOR通路是哺乳动物最重要的细胞内信号通路之一,对多种重要生理功能至关重要,包括细胞周期、细胞存活、蛋白质合成和生长、代谢、运动和血管生成,而38%的癌症患者中发现了 PI3K/AKT/mTOR 通路的改变,使其成为药物研发者开发药物的热点通路之一,包括PI3K、mTOR抑制剂均有药物获批上市。同时,该通路的过度活化广泛存在于各类癌种,包括乳腺癌、肺癌、头颈部肿瘤、子宫内膜癌、前列腺癌、结直肠癌等,潜在治疗市场空间广阔。
值得注意的是,AKT在PI3K/AKT/mTOR信号通路中处于核心位置,这个位置让AKTi对PIK3CA、AKT、 PTEN改变的患者都能获益,而PI3Ki只对PIK3CA突变患者有效。一方面对AKT抑制可以起到抑制肿瘤细胞增长的作用,另一方面,PI3K/AKT信号通路的活化可能导致多种小分子抑制剂的耐药和多类癌症的病情恶化,AKT抑制剂有望解决多类小分子抗癌药物的耐药问题。
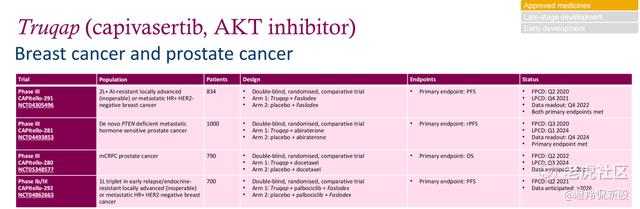
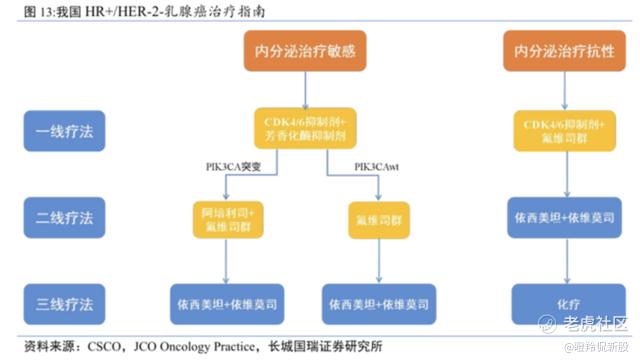
从阿斯利康的Truqap开启临床三期适应症范围看,集中在乳腺癌、前列腺癌两大领域,其中上述提到的局部晚期或转移性HR+/HER2-乳腺癌已经获批,在HR+/HER2-乳腺癌中,约40%-50%的患者存在PIK3CA/AKT1/PTEN等基因变异,导致AKT通路异常激活,引发内分泌治疗耐药,二线治疗的市场空间不俗。
前列腺癌领域,Truqap也取得了突破。针对PTEN缺陷的转移性激素敏感性前列腺癌(mHSPC)的CAPItello - 281三期取得了积极的结果,Truqap联合阿比特龙、ADT对比阿比特龙、ADT联合安慰剂在放射学无进展生存期(rPFS)的主要终点方面显示出统计学意义和临床意义上的改善,同时显示出总生存期(OS)改善的早期趋势(数据尚未成熟)。
全球每年新诊断20万名转移性前列腺癌,其中1/4患者存在PTEN缺陷,这类患者预后特别差。
Truqap更大的王炸,还在后头。
Truqap正在进行二线治疗转移性去势抵抗前列腺癌(mCRPC)的CAPItello-280三期研究和一线治疗晚期HR+/HER2-乳腺癌患者的CAPItello-292三期研究,均在2026年前后读出关键数据,如果两个早线适应症三期临床均获得成功,那么其将预定一个全球重磅炸弹的名额。
02
PI3K/AKT/mTOR通路上的重磅炸弹
PI3K/AKT/mTOR通路在过去出过一些重磅炸弹。
以mTOR抑制剂依维莫司为例,该药为一种广谱的抗肿瘤药物,曾在2019年达到20.24亿美元销售峰值,其获批的适应症非常广泛,包括晚期肾细胞癌、神经内分泌肿瘤、乳腺癌等。
如今,有望超越依维莫司的核心靶点抑制剂集中在PI3K、AKT这两大方向,前述AKT抑制剂Truqap美银美林预测峰值超过38亿美元,而罗氏预测PI3Kα抑制剂Inavolisib销售峰值潜力为23亿美元。
Truqap与Inavolisib两者最大的争锋市场,莫过于乳腺癌赛道。
从覆盖人群上看,数据显示约50%的HR+晚期乳腺癌患者携带PIK3CA、AKT1或PTEN基因的改变,而携带PIK3CA突变的HR+晚期乳腺癌约占40%,Truqap覆盖潜在患者规模可能更大。
再从最大块的市场(临床探索一线适应症的设计)来看,Truqap的CAPItello-292针对一线治疗晚期HR+/HER2-乳腺癌患者,而Inavolisib的携带PIK3CA突变的HR+/HER2-乳腺癌患者,前者不仅限于突变阳性患者,未来潜在市场空间可能更大。
再者据美银美林调研显示,Inavolisib仅用于一线快速进展人群(约占全体患者的10%),而Truqap的二线试验针对慢进展人群,约占二线人群的75%。
不过,两款创新分子均展现出优异的疗效,为乳腺癌患者提供了更好的临床获益。
Inavolisib在INAVO120研究(一线)中联合哌柏西利和氟维司群治疗的中位无进展生存期(PFS)为15.0个月,显著优于安慰剂组的7.3个月,疾病进展或死亡风险降低57%;
在既往接受过CDK4/6抑制剂治疗的HR+/HER2-晚期乳腺癌患者(二线)中,并伴有PIK3CA/AKT1/PTEN 通路改变的人群,“Truqap+氟维司群”治疗组与“安慰剂+氟维司群”对照组mPFS对比为7.3个月vs 3.1个月(HR=0.50)。
由此可见,PI3K/AKT/mTOR通路创新分子开发的市场潜力之大。
03
国内映射
谈到AKT抑制剂的国内映射,Truqap之外,来凯医药LAE002是全球仅有的两种处于或完成关键临床开发阶段的抗癌AKT抑制剂之一。
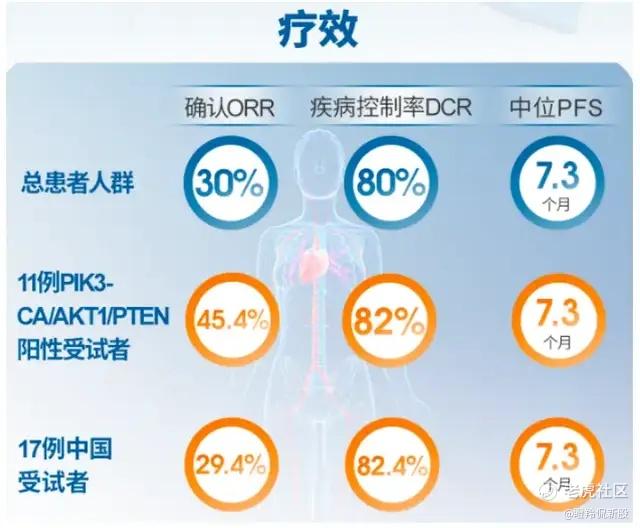
LAE002作为全球第二的AKT抑制剂管线,在早期的临床数据中看到了优于Truqap的积极讯号。2023 SABCS大会上,来凯医药公布了LAE002联合氟维司群治疗HR+/HER2-乳腺癌二线治疗1b期临床数据:在20位受试者中,全人群治疗组ORR为30%、DCR为80%、mPFS为7.3个月;在11例PIK3CA/AKT1/PTEN突变患者中,ORR为45.4%、DCR为82%、mPFS为7.3个月。
非头对头的数据比较上,LAE002小样本临床数据对比Capivasertib三期数据取得了更好的ORR,尤其在PIK3CA/AKT1/PTEN突变患者中,ORR的获益更加突出,这也符合LAE002临床前对AKT的抑制效力更强的数据。值得注意的是,两个临床CDK4/6经治耐药患者比例相差无几,基本验证了AKT抑制剂作为CDK4/6耐药后线治疗标准的潜力。
更惊艳的可能是LAE002表现出的安全性,亮点包括未出现因不良反应停用药物事件(Capivasertib有13.0%)、观察到的大多数不良事件为1级(未出现4级及以上安全事件)、临床中未进行剂量调整(Capivasertib有约20%患者调整)。
目前,LAE002在国内正处于HR+/HER2-乳腺癌伴随PIK3CA/AKT1/PTEN改变人群的关键三期临床,另外LAE002联合LAE001治疗转移性去势抵抗性前列腺癌(mCRPC)患者临床也获得了FDA的批准。
要看到来凯医药除了增肌减脂的LAE102之外,还有LAE002这样一个贡献估值的优秀分子。
至于PI3Kα抑制剂,国内进度较快的是翰森药业的HS-10352在2022AACR大会上,HS-10352公布了初步早期临床结果:在无标准治疗方案或无法获得或不能耐受标准治疗的HR+/HER2-晚期乳腺癌受试者中,显示出良好的安全性、耐受性和药代动力学(PK)特征,并观察到了初步的抗肿瘤活性,携带PIK3CA突变的人群中抗肿瘤活性更优。而另外早在2022年,君实生物以每个药物项目1.5亿元技术转让费获得了润佳医药2款药物的50%权益,其中就包括一款PI3Kα抑制剂(JS105)。
结语:尽管小分子药物的新技术蛋白降解在创新过程中遭遇荆棘,但我们在大量的慢病如减重、减脂领域看到了大量的研发者围绕热门靶点进行小分子药物的研发(如GLP-1、PCSK9等),或许这就是小分子药物研发久盛不衰的魅力之一(成本、患者依从性)。 $翰森制药(03692)$ $来凯医药-B(02105)$ $阿斯利康(AZN)$

精彩评论