现场反响热烈!2023ASH宜明昂科替达派西普(Timdarpacept)治疗cHL、MDS及CMML患者临床II期最新数据公布
$宜明昂科-B(01541)$ 2023年第65届美国血液学会年会(65th ASH Congress)于2023年12月9日至12日举行。由宜明昂科生物医药技术(上海)股份有限公司(简称“宜明昂科”,香港交易所股票代码:01541.HK)研发的,国内首个靶向人CD47的SIRPαFc融合蛋白药物替达派西普(药物编号: IMM01)共计三篇临床II期创新研究结果在2023年美国血液学会(ASH)年会入选口头报告及壁报展示。宜明昂科团队在ASH会议报告的临床研究结果得到了大会现场长时间的掌声,引起热烈反响,表明了与会者对宜明昂科替达派西普(药物编号: IMM01)临床表现的高度认可。
宜明昂科替达派西普(药物编号: IMM01)三篇临床II期创新研究结果入选2023美国血液学会(ASH)年会口头报告及壁报展示,其中两篇入选2023 ASH口头报告(分别是PD1抗体治疗失败后的cHL适应症及1线MDS适应症),另外一篇1线CMML适应症研究成果以壁报形式展示。这是该项目的临床进展连续2年入选ASH年会。
IMM01是中国首个进入临床阶段的SIRPα-Fc融合蛋白,正被开发用于与其他药物联合治疗多种血液肿瘤和实体瘤。凭借单药治疗临床试验中的初步有效性和良好的安全性,以及IMM01在此次ASH年会上展示的临床II期治疗cHL、MDS及CMML患者的数据再次证明,IMM01在与其它抗肿瘤药联用时具有强大的药物协同作用并可以提升疗效。
IMM01
Number
替达派西普入选2023 ASH年会的研究摘要如下:
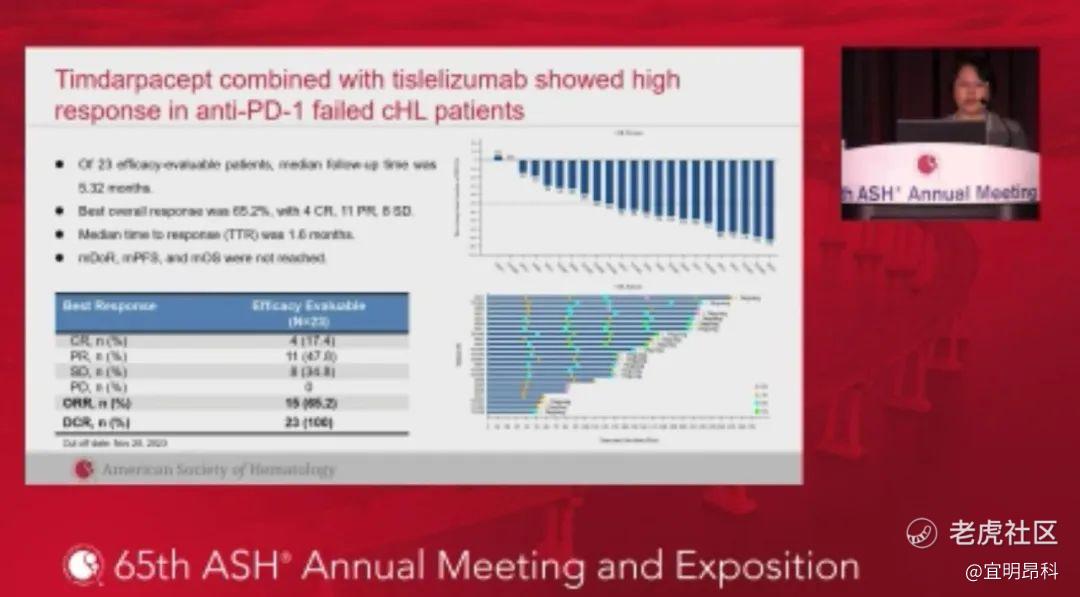
IMM01 Plus Tislelizumab in Prior Anti-PD-1 Failed Classic Hodgkin Lymphoma: An Open Label, Multicenter, Phase 2 Study (IMM01-04) Evaluating Safety As Well As Preliminary Anti-Tumor Activity

本次ASH 现场报告了更新数据,IMM01联合替雷利珠单抗治疗既往PD1抗体治疗失败后的cHL患者ORR达65.2%, CR 17.4%, DCR 100%,而且在各个亚组分析中均显示可以从联合治疗中获益。另外,IMM01联合替雷利珠单抗治疗耐受性良好,没有报告G4 血小板减少,也没有患者发生因为药物相关不良反应导致的永久停药情况。
,时长00:09
北京肿瘤医院的宋玉琴副院长现场做口头报告
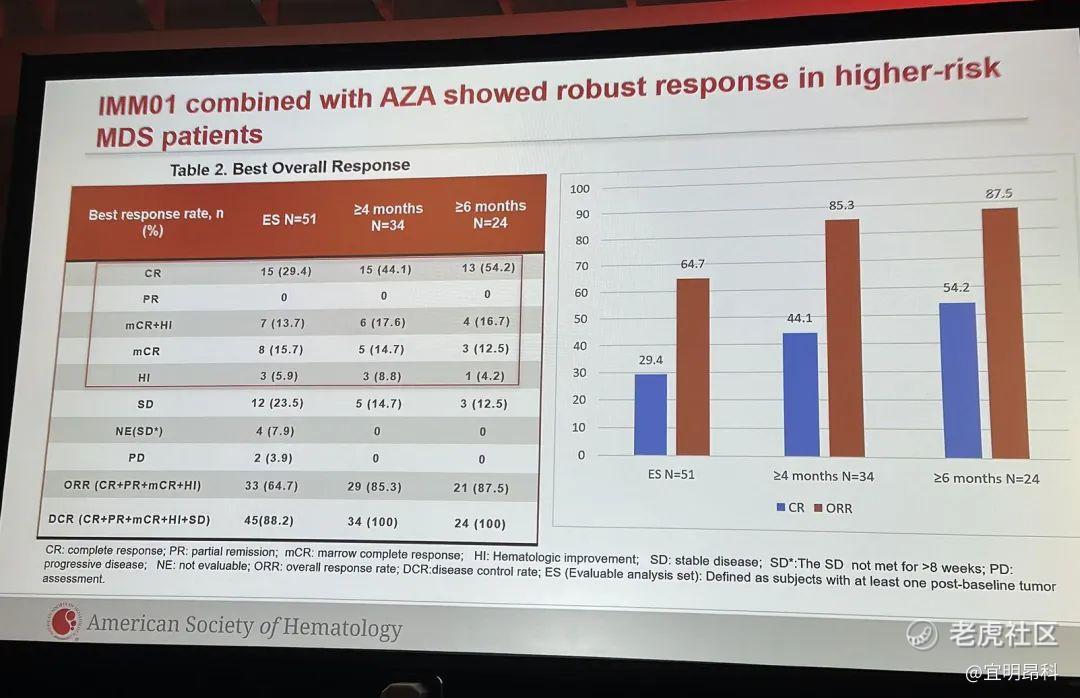
Preliminary Results of a Phase 2 Study of IMM01 Combined with Azacitidine (AZA) As the First-Line Treatment in Adult Patients with Higher Risk Myelodysplastic Syndromes (MDS)

本次ASH 现场报告了更新数据,IMM01联合AZA 治疗初治的中高危的MDS患者,ORR 64.7%,CRR 29.4%;治疗≥4个月的患者,ORR 达到85.3%,CRR 44.1%; 治疗超过≥6个月患者中, ORR达到87.5%, CRR 54.2%,疗效随着治疗时间延长而进一步提高。另外,IMM01联合AZA 治疗安全性良好,不需要采用低剂量预激处理,对比AZA单药治疗数据,联合治疗没有增加毒性,没有出现新的药物安全信号。
,时长00:16
中国医大一院的颜晓菁教授现场做口头报告
Preliminary Results of a Phase 2 Study of IMM01 Combined with Azacitidine (AZA) As the First-Line Treatment in Adult Patients with Chronic Myelomonocytic Leukemia (CMML)

本次ASH 现场报告了更新数据,IMM01联合AZA 治疗初治的CMML1-2患者,ORR 72.7%,CRR 27.3%;治疗≥4个月的患者,ORR 达到87.5%,CRR 37.3%; 治疗超过≥6个月患者中, ORR达到83.3%, CRR 41.7%,疗效随着治疗时间延长而进一步提高。另外,IMM01联合AZA 治疗安全性良好,不需要采用低剂量预激处理,对比AZA单药治疗数据,联合治疗没有增加毒性,没有出现新的药物安全信号。

宜明昂科创始人、董事长
田文志博士表示:
“一年一度的ASH年会是全球血液学领域规模最大的国际学术盛会之一,全面涵盖了血液疾病的病因研究和治疗研究。我们在ASH 2023大会上展示的研究结果,有利于让业界了解IMM01最新临床开发的研究数据。此次,IMM01多项研究入选口头报告或壁报展示及大会现场的热烈反响,体现了国际血液学界对IMM01的高度认可。由于我们药物分子的差异化设计,使得IMM01在体外实验中显示完全不与红细胞结合,不会引起严重贫血事件。同时由于糖基化修饰,大大降低了药物的免疫原性,改善了药物动力学参数,显著提高了药物的生物利用度。尤为重要的是在已经入组的初治的中高危的MDS患者、初治的CMML患者、初治的AML患者,以及既往PD1抗体治疗失败后的cHL患者中,均观察到令人振奋的疗效和良好的耐受性。此外,在这几个瘤种中均已观察到多个完全缓解的患者,有望给患者带来长期生存的机会。我们很高兴能有机会与肿瘤领域的同行们分享这些数据,并期待IMM01更多的临床数据进一步发布。”
宜明昂科首席医学官/高级副总裁
卢启应医师表示:
“IMM01 产品3个临床II期研究结果再次获得了今年ASH认可和肯定,2篇被ASH 接受为口头报告,1篇作为壁报展示。在ASH 现场,IMM01数据披露获得了现场热烈的关注。另外,我们还在ASH现场和来自美国著名肿瘤中心的白血病和淋巴瘤的顶尖教授分别会谈,均获得了专家浓厚的兴趣。我们期待快速地推进IMM01产品的临床开发,为广大肿瘤患者治疗带来全新的治疗选择,解决未满足的临床需求。”
关于IMM01
IMM01是基于宜明昂科自有研发平台研发、经基因修饰,并具有全球自主知识产权的新一代CD47靶向分子。IMM01具有双重机制,能够同时阻断来自肿瘤的“别吃我”信号,并通过IgG1激活患者免疫系统的“吃我”信号。IMM01在体内具有强大的抗肿瘤活性,临床上可以观察到单药的有效性。同时,在临床前体内药效试验中,IMM01与靶向药物或免疫治疗药物联用,显示了针对血液肿瘤还有实体瘤的强大的抑瘤活性。IMM01完美解决了CD47靶点药物研发中的核心痛点,相比之下具有较大的差异化优势,并具有“Best-In-Class”的潜力。IMM01目前已分别在中国、日本、美国和欧盟获批发明专利。
关于宜明昂科

宜明昂科生物医药技术(上海)股份有限公司于2015年6月在中国(上海)自由贸易试验区张江高科科技园区成立。我们是一家以科研为导向的生物技术公司,致力于开发肿瘤免疫疗法。我们是全球少数能够对先天性免疫和适应性免疫进行系统性利用的生物技术公司之一。目前获批的免疫疗法主要专注于适应性免疫系统,且由于在许多癌症适应症的低响应率及不可避免的耐药性及╱或复发,经常面临有限的临床获益。利用先天和适应性免疫系统使我们能够克服当前基于T细胞的免疫疗法的局限性,并解决癌症患者大量未被满足的医疗需求。
我们曾获“第二届生物科技创新50企业榜单”、“药物创新济世奖”、“2021中国医药创新种子企业100强”、“2020年度浦东新区创新创业20强”、“高新技术企业证书”、“2019中国生物医药最具创新力50强企业”、“张江创投百强企业荣誉称号”等。
2023年9月5日,宜明昂科在香港联合交易所正式挂牌上市,股票代码:01541.HK。
前瞻性声明
本新闻稿有若干前瞻性陈述,该等前瞻性陈述并非历史事实,乃基于宜明昂科的现有看法、假设和期待而对未来事件做出的预测,通常会使用“将”、“可能”、“期望”、“相信”、“计划”、“预估”、“预测“及其他类似词语进行表述。尽管本公司相信所做的预测合理,但是基于未来事件固有的不确定性,我们的实际未来业绩或表现可能与预测有重大差异。因此,您应注意,依赖任何前瞻性陈述可能导致已知及未知的重大风险和不确定性。本新闻稿载有的所有前瞻性陈述需参照本部分所列的提示声明。本新闻稿所载的所有信息仅以截至本新闻稿做出当日为准,且仅基于当日的假设,除法律有所规定外,本公司概不承担义务对该等前瞻性陈述更新。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。


