群芳争艳丨坚持走小分子的和誉凌寒独自开
转自:祎枕黄粱
和誉医药成立于2016年,目标是解决中国及全球患者未获满足的迫切需求。 $和誉-B(02256)$
管理团队经验丰富且国际化
创始人是徐耀昌博士与俞红平博士,其中徐博士有着40年的医药经验。二人都在翰森生物医药科技有限公司任职过,搭建了翰森的研发团队与研发体系,有过成功的开发EGFR突变靶点(阿美替尼)的经验。并且既往都有着跨国药企的经历,徐博士是第一位进入礼来新药研发管理层的华人。
此外首席财务官,首席医学官,CMC副总裁均有着丰富的跨国药企经验。HR副总裁负责过蚂蚁集团国际业务产品技术部HR负责人。整体管理团队资历深厚,经验丰富,具有国内外企业管理经验。
研发管线
目前处于临床阶段的管线分为两部分 靶向肿瘤与免疫肿瘤。可以看出,目前和誉主要研发方向在舒适区肿瘤领域,这也是创始人有着丰富成功经验的领域。
其中靶向肿瘤方向有CSF-1R,FGFR4,Pan-FGFR,GFR 2/3,GFR耐药突变,EGFR exon20,EGFR C797s,PRMTSMTA免疫肿瘤方向有口服PD-L1,CXCR4,CD73。
管线其实反映了创始人的性格,因为他们创造了中国首个EGFR 酪氨酸激酶抑制剂阿美替尼,所以相较于大分子单抗药物,和誉医药格外倾心于小分子抗肿瘤药物。目前研发进度最快的药物包含CSF-1R抑制剂ABSK021,FGFR4抑制剂ABSK011,泛FGFR抑制剂ABSK091,CXCR4抑制剂ABSK081。
尝试了解一下四大金刚的靶点与潜力。
CSF-1R抑制剂ABSK021
这是一个获得MNC默克认可的靶点及药物。7000万美金的首付,全球行权费用8500万美元,潜在总价值高达6亿美金。后续和誉可以获得全年净销售额的两位数比例提成。核心适应症腱鞘巨细胞瘤(TGCT)。
TGCT是一种局部侵袭性肿瘤,目前治疗手段有限,手术切除后也容易复发。021的全球III期MANEUVER研究取得了积极的关键结果:在第25周时,匹米替尼组的客观缓解率(ORR)达到54.0%,远高于安慰剂组的3.2%,并且统计学差异显著(p<0.0001)。同时,每日一次口服匹米替尼的耐受性良好,因治疗相关不良事件而终止治疗的比例非常低,研究中未观察到胆汁淤积性肝毒性的证据。
此外,021还有慢性移植物抗宿主病与实体瘤适应症布局。
FGFR4抑制剂ABSK011
FGF19+肝癌的联合治疗与单药治疗。在肝癌的发生中,该通路的异常激活可能是癌变的关键驱动因素,整体FGF19蛋白过表达发生率约为10%~30%。通过四条信号通路促进细胞增殖,抑制细胞凋亡,促进上皮-间质转化等行为促进肿瘤发生。
肝癌在后线治疗中药物治疗模式缺乏,存在巨大的临床需求,一直以来,肝癌没有精确的靶向药使用。依帕戈替尼作为一款精准地靶向FGFR4的抑制剂,有望成为国内首款上市的肝癌靶向药。真正的FIC。
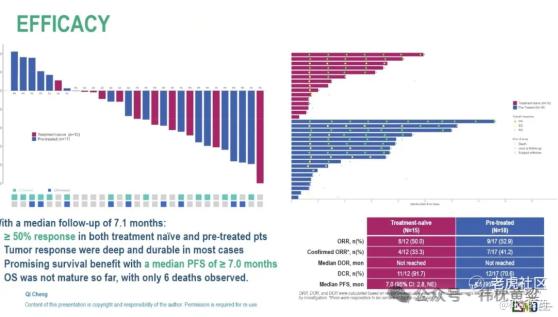
2025 ESMO GI会议中,报道了依帕戈替尼联合阿替利珠单抗治疗既往未经治与经治FGF19+肝癌患者,研究数据显示:经治患者(100%免疫经治)展现出卓越的疗效,ORR高达52.9%,mPFS 8.3个月。初治患者疗效数据显示:ORR为50%,确认的ORR 33.3%,mPFS为7个月。
泛FGFR抑制剂ABSK091
布局尿路上皮癌与其他实体瘤。Fexagratinib(Fexa, AZD4547)作为一种强效且具有选择性的FGFR抑制剂,已在具有FGFR突变的mUC患者中显示出抗肿瘤活性,II期研究(ABSK091-203,NCT05775874)旨在评估Fexagratinib与替雷利珠单抗联合治疗在拒绝或不耐受一线铂类化疗的FGFRa mUC患者中的疗效。
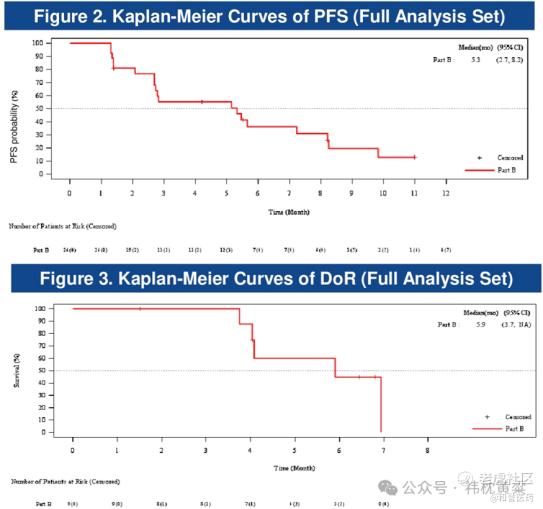
在疗效方面,在24名可评估患者中,9例(37.5%)获得了部分缓解(PR)。在具有FGFR3过表达但无突变融合的可评估患者中,ORR为37.5%(6/16)。治疗的中位无进展生存期(mPFS)为5.3个月(95%CI: 2.7-8.2),中位缓解持续时间(mDoR)为5.9个月(95%CI: 3.7, NA)。中规中矩的数据表现。
联合疗法在FGFR3过表达且无突变融合或PD-L1阴性的mUC患者中疗效显著,同时可能对于FGFR3 mRNA过表达合并FGFR3基因突变的患者提供更大获益同一Class的竞品厄达替尼3期THOR临床研究显示:中位随访15.9个月时,厄达替尼组和化疗组治疗FGFR3基因突变UC中位总生存期分别为12.1个月和7.8个月;中位无进展生存分别为5.6个月和2.7个月。相比化疗组,厄达替尼组死亡和疾病进展风险分别降低36%和42%。可以看出ABSK091联合替雷利珠单抗跟厄达替尼疗效数据相似。
膀胱癌是中国男性十大常见肿瘤之一,其中最常见的类型是尿路上皮癌,约占90%。约有20%的转移性尿路上皮癌患者携带FGFR基因变异。2022年中国新发膀胱癌患者7.32万人,整体FGFR基因突变患者约为1.3w人。
CXCR4抑制剂ABSK081
布局适应症:TNBC与疣,低丙种球蛋白血症,感染及骨髓粒细胞缺乏症ABSK081由和誉医药从X4 Pharmaceuticals引进而来,是一款全球领先的FIC口服CXCR4拮抗剂,用于治疗经基因证实的WHIM综合征,一种由CXCR4基因功能突变引起的原发性免疫缺陷疾病,关键临床III期试验显示,与安慰剂组相比,ABSK081组的年化感染率降低了约60% (p<0.01),经历严重感染(3 级或更高)的个人百分比减少75%以上,且感染平均总天数减少70%以上,显示出更具统计和临床意义的优势。
和誉拥有其在大中华地区肿瘤及WHIM适应症的商业化权益,并将主导其大中华地区多个肿瘤适应症的临床与商业开发。目前,ABSK081联合PD-1特瑞珠单抗治疗三阴性乳腺癌(TNBC)正在临床I/II期中。
像PD-L1口服药这类,除非是双抗AK112领头的这类药物持续失败,可能关注点才会由双抗转为PD-L1/PD-1,进而关注到口服药物。但是我觉得可能性比较低,哪怕是HARMONi研究OS报阴性,我仍然坚定看好可见的未来短时间内,双抗与ADC及其联合用药是未来。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。