超20亿元:年内规模最大的药企IPO诞生
2025年9月,在生物医药领域,有1家公司采取IPO形式上市,1家公司通过SPAC合并上市,1家公司以转板形式上市。
一、IPO上市
9月,仅有1家公司生物医药公司以IPO的方式赴美上市,市场非常清淡。
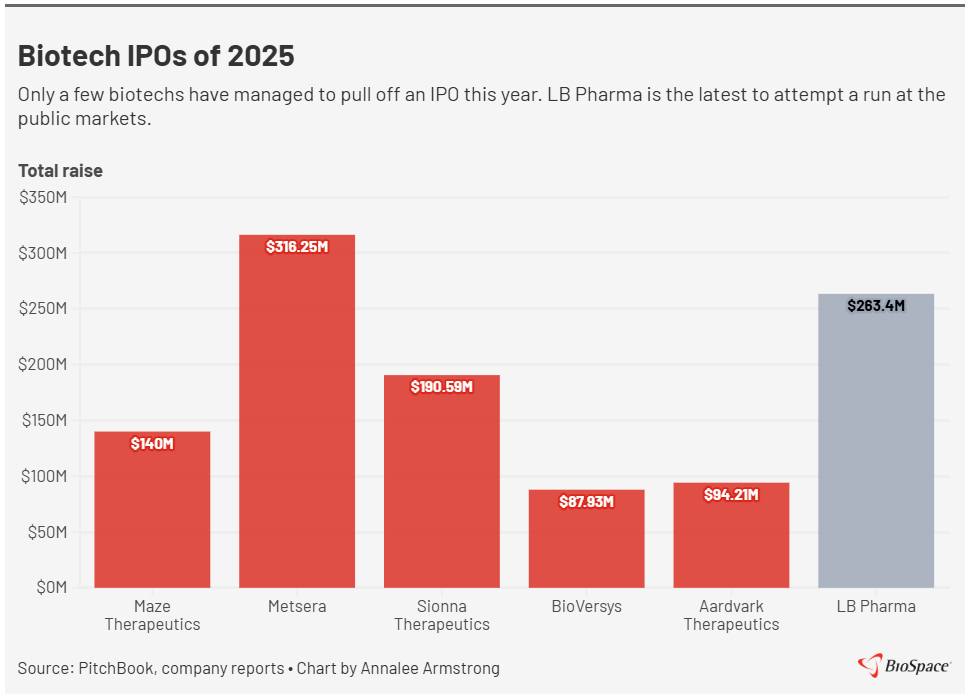
但从募集规模来看,LB Pharmaceuticals却是今年以来规模最大的生物医药IPO,超过了1月上市的Metsera(2.75亿美元)与2月上市的Sionna Therapeutics(1.9亿美元)。
1、LB Pharmaceuticals(NASDAQ:LBRX)
9月10日,LB Pharmaceuticals在纳斯达克交易所上市,发行价为每股15美元,发行1900万股,融资规模达2.85亿美元,打破了打破了生物科技行业长达7个月的5000万美元以上IPO的僵局。
LB Pharmaceuticals成立于2023年,是一家专注于中枢神经系统的生命科学公司,致力于将在其他国家或地区已成功应用、但在美国尚未上市的改良型中枢神经系统疾病治疗药物进行商业化。
与其他管线丰富的生物医药公司不同,LB Pharmaceuticals仅有一款药物:LB-102。LB-102是一种新型多巴胺/7型五羟色胺受体拮抗剂,它以氨磺必利(amisulpride)为基础。
氨磺必利是是一款四十多年前开发的实际作用于D2、D3、5-HT7的多巴胺拮抗剂,用于治疗精神分裂症,已在50多个国家(不包括美国)获得批准。氨磺必利的局限性在于血脑屏障穿透率很低,临床剂量因此高达 400-800mg/日,且高剂量也必然带来大量副作用,同时难以开发长效注射剂(LAI)。简言之,氨磺必利的劣势与当下药物“长周期、低剂量、少副作用”的趋势背道而驰。
通过苯甲酰胺环 N-位单甲基化,公司药物LB-102实现了三重优化:
血脑屏障透过率提升约 10 倍(PET 脑摄取研究);
维持对 D2/D3/5-HT7 受体的高亲和力与选择性;
允许每日一次口服(50-100 mg),剂量较母体降低 75%-87.5%,有望减少高催乳素血症与 QT延长风险。
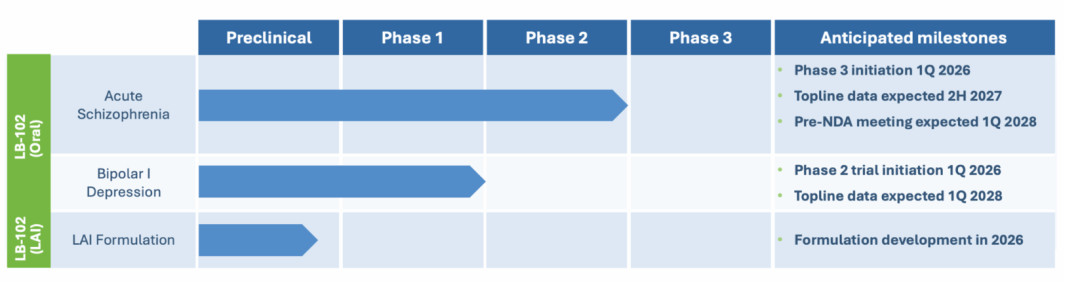
临床试验方面,2025年初,公司宣布其研发的潜在“first-in-class”药物LB-102在临床二期试验中成功达到主要终点,将进入关键的临床三期试验。数据显示,主要终点PANSS总分4周改善显著,安全性与母药类似,无EPS信号。
此外,公司还在研究LB-102的替代长效注射(LAI)制剂,有潜力为精神分裂症和双相抑郁症患者提供更好的临床结果和治疗依从性。
公司CEOHeather Turner之前曾担任Carmot Therapeutics的总裁兼首席执行官(被罗氏以31亿美元收购)、Lyell Immunopharma的首席法律总顾问兼秘书、Sangamo Therapeutics的执行副总裁、Atara的执行副总裁、Orexigen的总法律顾问兼秘书。
公司创始人兼董事Dr. Jeffrey Lieberman是精神神经病学领域的泰斗级人物,他不仅是哥伦比亚大学精神病学系前主任,也是纽约州精神病研究所前所长。
自成立以来,LB Pharma累计融资超4亿美元,投资者阵容豪华,包括Frazier Life Sciences、Deep Track Capital等知名机构。
二、SPAC上市
9月,有1家生物医药公司完成与SPAC公司的合并上市。
1、Semnur(PINK:SMNR)
9月23日,Semnur Pharmaceuticals完成与SPAC公司DECA合并上市,合并估值约25亿美元。合并后公司将在纳斯达克上市,股票代码为“SMNR”。
Semnur Pharmaceuticals是一家临床后期非阿片类镇痛药研发公司,是Scilex Holding(NASDAQ:SCLX)的全资子公司。
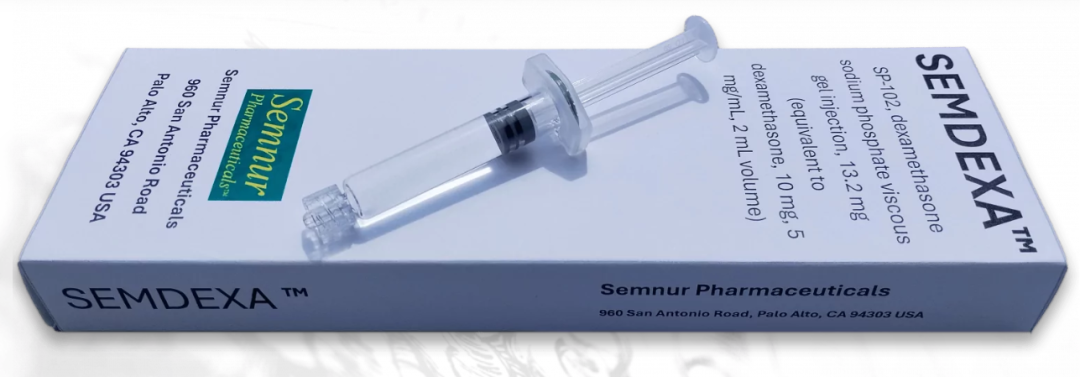
Semnur Pharmaceuticals的核心产品SP‑102(商品名 SEMDEXA™)是一种不含防腐剂、表面活性剂和颗粒物的地塞米松黏稠凝胶,针对慢性腰椎神经痛(sciatica)展开ESI(硬膜外类固醇注射)治疗方式。
此前,SP‑102作为硬膜外注射剂在临床三期试验中表现出安全性良好、疗效显著的潜力,安全性与安慰剂组对等并无严重不良事件,FDA已授予其 快速通道批准资格,目前正在推进regulatory filing准备,有望填补了当前无注射型非阿片类获批药空白。基于Syneos预测,SP‑102的第五年峰值年销售收入可达1.5–2亿美元。
值得注意的是,Semnur Pharmaceuticals的母公司ScilexHolding也是在2023年与SPAC公司FLAC合并上市,而Scilex Holding的母公司则是在华裔生物医药领域小有名气的Sorrento(NASDAQ:SRNE)。
三、反向并购上市(Reverse Merger)
9月,有1家公司宣布反向并购上市。
1、Barinthus(NASDAQ:BRNS)
9月30日,Clywedog Therapeutics宣布与Barinthus(NASDAQ:BRNS)反向并购上市,完成借壳后,上市公司代码为“CLYD”。根据合并协议,Barinthus Bio的股东预计将拥有合并后公司约34%的股份,Clywedog的股东预计将拥有合并后公司约66%的股份。
Clywedog Therapeutics是一家由OrbiMed与Torrey Pines Investment支持孵化设立的代谢领域的生物医药公司。
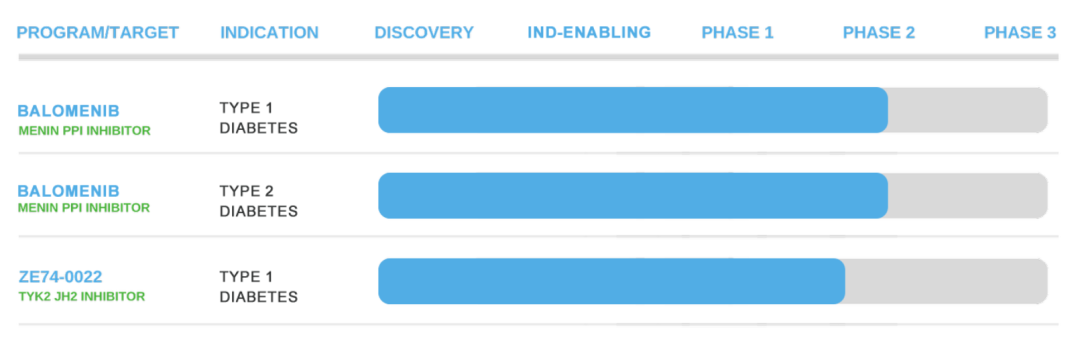
公司在研管线将包括三个具有广泛潜力的资产:用于治疗代谢和自身免疫性疾病,最初的重点是1型糖尿病(“T1D”),2型糖尿病(“T2D”)和乳糜泻的三个正在进行的项目。
CLY-101 (Balomenib):具有长期控制T2D血糖和恢复T1D胰岛素生成的潜力。通过可逆的蛋白-蛋白相互作用抑制menin, CLY101刺激负责多种血糖调节激素(包括胰岛素和胰高血糖素)分泌的胰岛再生,以改善胰岛素的新生生成。由于GLP-1受体表达增加,Balomenib有可能与GLP-1激动剂协同作用,并通过血糖控制和体重管理为糖尿病管理提供全面的方法。
目前,Balomenib完成的临床1期研究证明了健康志愿者的安全性和耐受性,提供了PK/PD数据,支持治疗T1D和T2D下一步试验。2型糖尿病患者的临床2A期原理证明研究预计将于2026年下半年公布。1型糖尿病(临床三期)患者的2A期原理证明研究预计将于2026年下半年公布。
CLY-201:一款高选择性TYK2抑制剂,靶向t细胞介导的炎症,可破坏胰岛素分泌的胰腺β细胞,这是T1D的潜在原因,可阻止导致1型糖尿病的炎症。
目前,临床一期单次和多次递增剂量研究(SAD/MAD)在健康志愿者中完成,在预计显示有效的暴露水平下没有明显的不良事件。公司计划对1型糖尿病(2期)患者进行2期研究,以评估安全性、血糖控制和循环c肽水平。
VTP-1000:一款高分化抗原特异性耐受免疫疗法,用于预防或减轻乳糜泻患者接触谷蛋白后的症状
目前,6名患者中有5名入组了AVALON研究临床一期研究试验。AVALON 临床一期研究的SAD部分预计将于2025年第四季度发布,AVALON第一阶段MAD部分数据预计将于2026年中期发布。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。