远大医药创新RDC产品ITM-11的NDA获得美国FDA正式受理
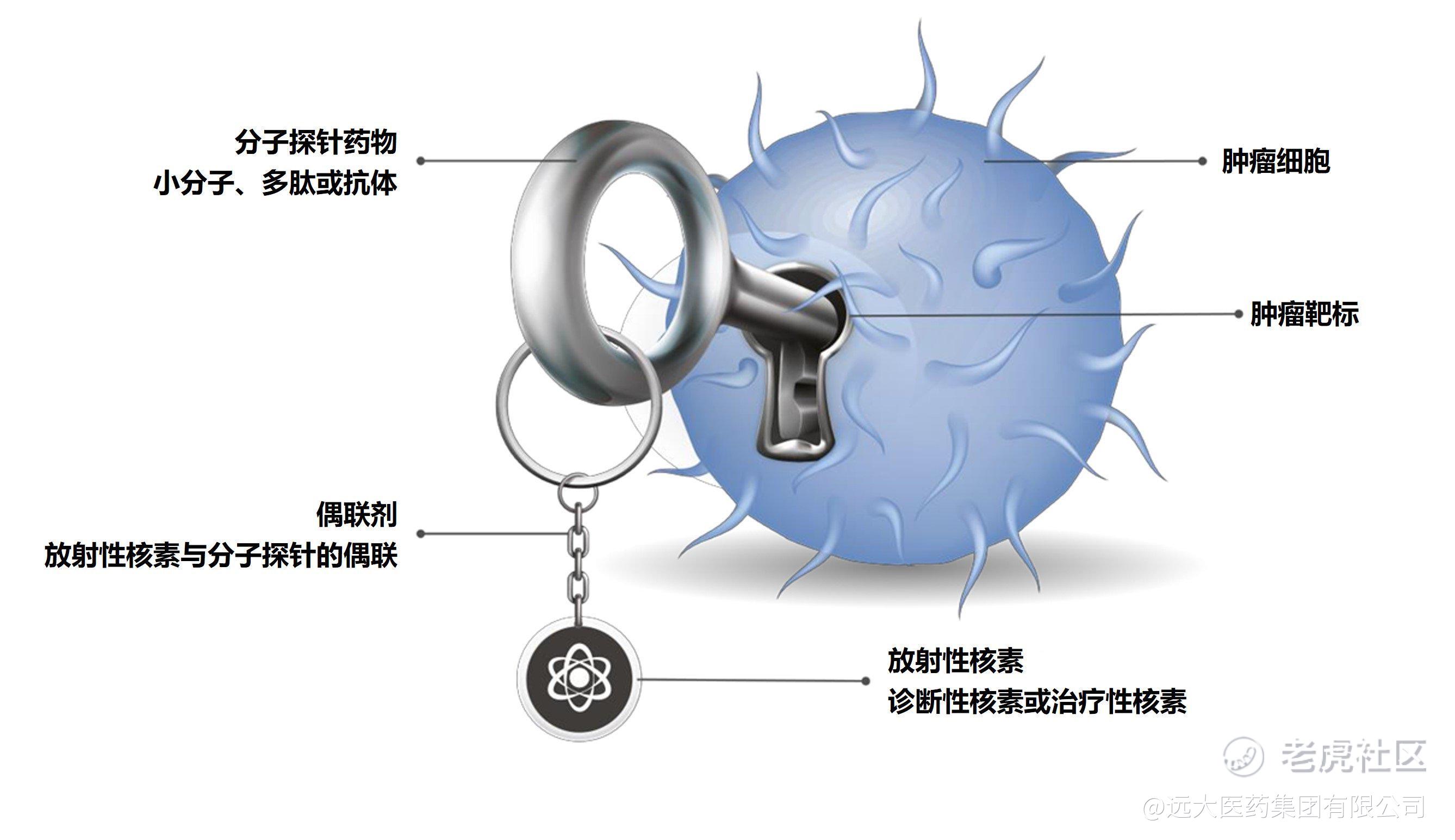
· ITM-11是一款基于放射性核素偶联技术靶向杀伤治疗GEP-NETs的RDC产品,该产品是将无载体177Lu与生长抑素类似物偶联,通过与GEP-NETs表面高水平表达的SSTR结合杀伤肿瘤细胞;
· ITM-11中的无载体177Lu拥有更高的比活度和纯度、杂质更少、半衰期更长等优点,使得放射性废物更易于处理[1],ITM-11已经获得美国FDA和欧洲EMA的孤儿药资格;
· ITM-11可与本集团引进的另一款用于诊断GEP-NETs的RDC产品ITM-14D形成产品组合,实现对GEP-NETs的诊疗一体化。
近日,远大医药(0512.HK)在放射性核素偶联(RDC)领域的重要战略合作伙伴ITM Isotope Technologies Munich SE (ITM SE)宣布了用于治疗胃肠胰腺神经内分泌瘤(GEP-NETs)的创新RDC产品ITM-11的新药上市申请(NDA)获得美国FDA正式受理。
此前,本集团于2021年12月与ITM SE签署了产品战略合作协议,并获得其开发的包括ITM-11及ITM-14D (TOCscan®)在内的三款创新RDC产品在大中华区(中国大陆、中国香港特别行政区、中国澳门特别行政区、中国台湾地区)的独家开发、生产及商业化权益。
ITM-11已获美国及欧洲孤儿药认定,或实现GEP-NETs各阶段病程全覆盖
关于ITM-11及其临床试验:
ITM-11是一款基于放射性核素偶联技术靶向杀伤治疗GEP-NETs的RDC产品,该产品是将无载体177Lu与生长抑素类似物偶联,通过与GEP-NETs表面高水平表达的生长抑素受体(SSTR)结合杀伤肿瘤细胞。与有载体177Lu相比,ITM-11中的无载体177Lu拥有更高的比活度和纯度、杂质更少、半衰期更长等优点,使得放射性废物更易于处理[1]。ITM-11已经获得美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)的孤儿药资格。
本次ITM-11美国NDA申报是基于其海外III期COMPETE试验的结果。该试验是一项前瞻性、随机、对照、开放标签研究,纳入了309例无法手术切除的进展性1级或2级GEP-NETs患者。COMPETE试验达到了主要终点,结果显示,与靶向分子治疗药物依维莫司相比,接受ITM-11治疗的患者的中位无进展生存期 (mPFS) 显著延长;同时,接受ITM-11治疗的患者的客观缓解率 (ORR) 也显著高于依维莫司治疗的患者[2]。
国内研究方面,2025年3月,ITM-11在中国加入的国际多中心III期临床试验(COMPOSE试验)完成了首例患者入组给药。COMPOSE试验是一项前瞻性、随机、对照、开放标签、国际多中心的III期临床试验,拟在中国、美国、英国、法国、德国、澳大利亚等全球11个国家入组约250名患者,旨在评估ITM-11与最佳标准治疗相比,在高分化侵袭性2级和3级、生长抑素受体阳性(SSTR+)GEP-NETs患者中的有效性和安全性。目前,该试验正在顺利推进中。
此外,本集团于2024年12月获得国家药监局批准在中国开展另一项ITM-11的III期临床试验(COMPETE桥接试验),旨在评估ITM-11多肽受体放射性核素治疗(PRRT)对比标准治疗,在不可手术、进展性、高分化1级或2级、SSTR+的GEP-NETs患者中的有效性和安全性。COMPETE桥接试验旨在扩大ITM-11产品的潜在适用人群至中国患者,并实现ITM-11在GEP-NETs各阶段病程的全方位覆盖。
关于胃肠胰腺神经内分泌瘤:
根据Frost & Sullivan的数据,2020年,中国胃肠胰腺神经内分泌瘤的新发确诊病例为71,300例,发病率逐年上升。《CSCO神经内分泌肿瘤诊疗指南2021》中提示,基于177Lu的肽受体放射性核素治疗在无进展生存时间(PFS)和客观缓解率(ORR)等指标方面优于目前临床一线使用的高剂量奥曲肽(生长抑素类似物)。
ITM-11可与本集团引进的另一款用于诊断GEP-NETs的RDC产品ITM-14D形成产品组合,实现对GEP-NETs的诊疗一体化,本集团期望以此为中国GEP-NETs患者提供全新的诊疗方案。
持续推进创新产品研发,夯实全球核药领军地位
本集团在核药抗肿瘤诊疗板块已实现了研发、生产、配送、销售等多个环节的全方位布局,板块全球员工超过900人,以波士顿、成都为核心的研发基地,波士顿、法兰克福、新加坡、成都所在的生产基地以及覆盖全球50多个国家和地区的销售网络为基础,本集团已实现了全球化的核药产业链布局。
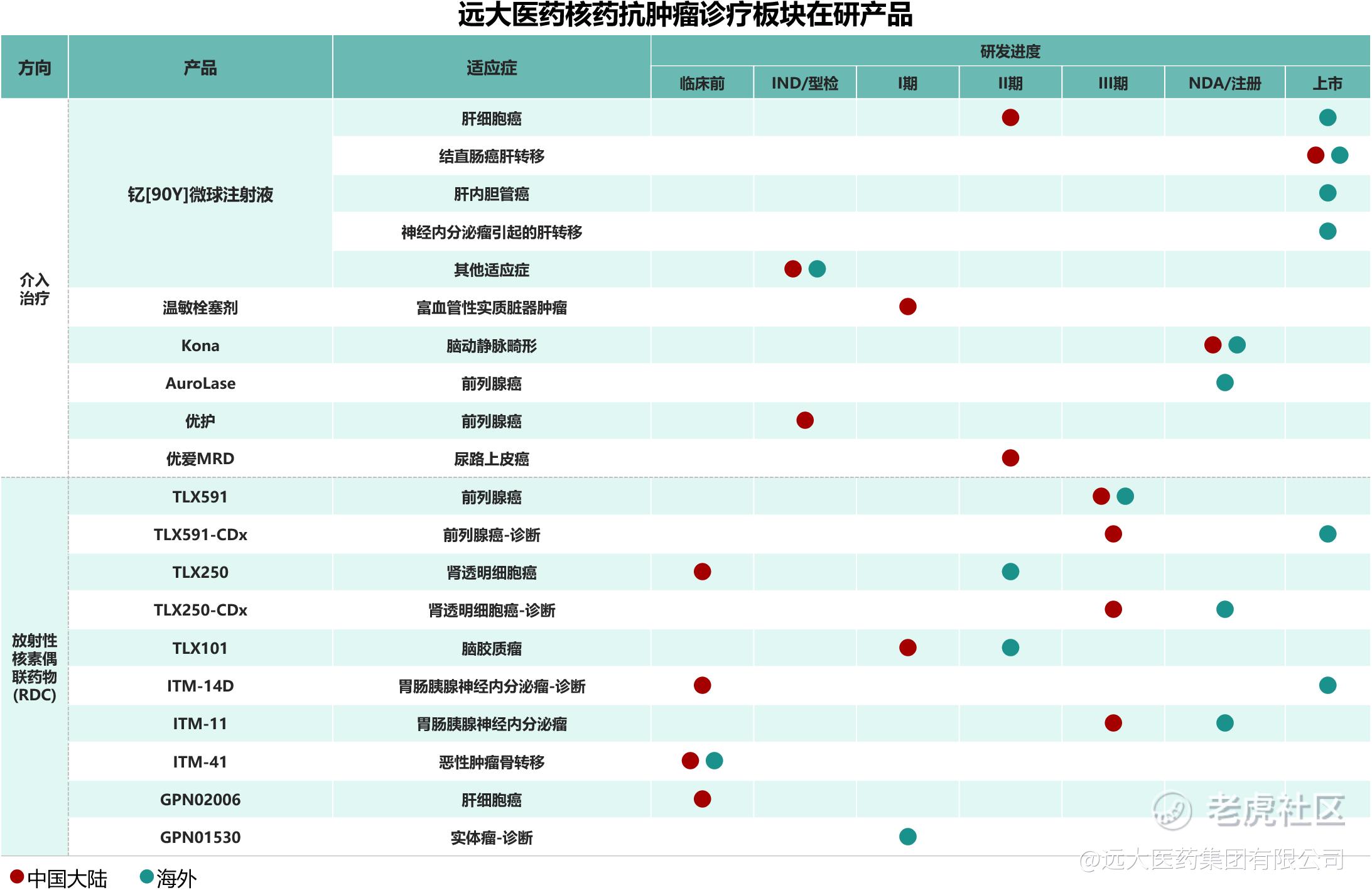
本集团联合Sirtex Medical Pty Ltd并与Telix Pharmaceuticals Limited (ASX: TLX; NASDAQ: TLX)和ITM SE合作,搭建了具有国际化一流水平的肿瘤介入研发平台和放射性核素偶联药物(RDC)研发平台。围绕肿瘤诊疗一体化的治疗理念,目前在研发注册阶段已储备16款创新产品,涵盖68Ga、177Lu、131I、90Y、89Zr在内的5种放射性核素,覆盖了肝癌、前列腺癌、脑癌等在内的7个癌种;早期研发阶段以RDC药物为主,产品储备10余款。在产品种类方面,涵盖诊断和治疗两类核素药物,为患者提供多适应症治疗选择、多手段且诊疗一体化的全球领先的抗肿瘤方案。[3]
板块内创新产品全球研发工作顺利推进。中国方面,易甘泰®钇[90Y]微球注射液于2022年1月顺利上市,用于治疗结直肠癌肝转移,并于2025年5月获得中国药监局批准开展治疗不可切除HCC的II期注册性临床试验;全球创新温度敏感性栓塞剂GPN00289于2025年10月完成了注册性临床研究的全部患者入组。海外注册方面,SIR-Spheres®钇[90Y]微球注射液(易甘泰®)于2025年7月在美国提前正式获批新适应症,用于治疗不可切除HCC,标志着SIR-Spheres®钇[90Y]微球注射液成为全球首个且唯一获FDA批准用于不可切除HCC和结直肠癌肝转移双重适应症的选择性内放射治疗产品;于2025年9月获欧洲CE标志认证新增多种肝癌适应症,进一步推动该产品在不可切除肝癌治疗领域的全方位覆盖,实现市场空间战略级扩容,充分彰显本集团优秀的海外临床注册与商业化运营能力,为后续自研创新核药产品的全球开发提供重要保障;同时,相关海外临床数据也将为该产品在中国拓展肝癌相关适应症提供关键支持;此外,本集团正携手中外专家合作开发钇[90Y]微球注射液的其他适应症,并将采用“中美双报”的国际化注册路径,加速该产品的全球市场拓展。
目前,本集团在核药抗肿瘤诊疗板块已有五款创新RDC获批开展注册性临床研究,其中四款已进入III期临床阶段,包括诊断前列腺癌的产品TLX591-CDx、治疗前列腺癌的产品TLX591、诊断透明细胞肾细胞癌产品TLX250-CDx以及治疗胃肠胰腺神经内分泌瘤(GEP-NETs)的产品ITM-11。此外,全球创新、基于放射性核素-抗体偶联技术的靶向磷脂酰肌醇蛋白聚糖3 (GPC-3)的诊断型放射性药物GPN02006早前在中国开展的研究者发起的临床研究(IIT临床研究)取得了里程碑式突破,并在2025年北美核医学与分子影像学会(SNMMI)年会斩获口头报告,该产品极具潜力,有望成为全球首个针对GPC-3靶点的肝细胞癌(HCC)诊断类RDC产品。截至目前,本集团是进入中国III期临床研究中诊断和治疗类RDC创新药总计储备最多的企业,也是全球范围内在核药抗肿瘤领域拥有最丰富产品管线和诊疗一体化布局的创新药企之一[3]。
关于本集团成都核药研发及生产基地:
本集团位于中国四川省成都市温江区的远大医药放射性药物研发及生产基地已于2025年4月竣工验收,5月获得国家生态环境部颁发的甲级《辐射安全许可证》,6月底正式投入运营。该基地为全球首个核药全产业链闭环平台,覆盖“同位素制备–核药研发–生产临床–商业化”全链条,形成从早期研发到临床转化到上市销售的全生命周期管理能力,研发效率国际领先;解决了核药“卡脖子”难题,100%自主生产破解进口依赖困局,14条高标准GMP生产线实现多品种、规模化制备需求;建立全流程智能管理体系,核电级安全与无人化智造,可实现辐射“零泄漏”,污染“零外排”,职业照射“零超标”,达到全球顶尖核设施标准;建立世界一流研发生产质量与运营体系,是目前国际范围内核素种类最全、自动化程度最高的智能工厂之一。该研发及生产基地将进一步夯实本集团核药产业的基础,加速全球创新研发管线的落地,推动本集团实现核药产业的高质量发展,培育高价值重磅品种,为本集团放射性药物的国产化落地奠定坚实的基础。
未来,本集团将持续加强核药抗肿瘤诊疗板块的研发和建设,丰富和完善产品管线及产业布局,形成以易甘泰®钇[90Y]微球注射液为核心的核药抗肿瘤诊疗产品集群,持续夯实本集团在全球核药抗肿瘤诊疗领域领军企业地位。
远大医药集团有限公司董事会表示:“本集团一直高度重视创新产品和先进技术的研发,以患者需求为核心,以科技创新为驱动,针对尚未满足的临床需求,加大对全球创新产品和先进技术的投入,丰富和完善产品管线及产业布局,采用‘全球化运营布局,双循环经营发展’策略,形成国内国际双循环联动发展并相互促进的新格局,充分发挥本集团的产业优势和研发实力,快速将科技创新产品落地上市,为全球患者提供更先进更多样的治疗方案。”
[1]根据现有公开信息;
[2]数据来源于COMPETE试验结果;
[3]研发风险提示:文中提及的在研产品尚未获得上市批准,其安全性和有效性需经完整临床研究及监管审批确认,不构成任何治疗承诺或商业推广。对在研产品上市时间的任何预期仅为基于当前情况进行初步判断的前瞻性表述,具有相当风险和不确定性。
前瞻性声明:
本新闻稿旨在分享本集团业务相关动态及进展,仅供医疗卫生专业人士参阅,非广告用途。本新闻稿信息仅供参考,不作为诊疗依据,如有身体不适请及时就医,本集团不对任何药品和/或适应症作推荐。
本新闻稿中可能会包含某些前瞻性表述。这些表述本质上具有相当风险和不确定性。在使用“预期”、“相信”、“预测”、“期望”、“打算”及其他类似词语进行表述时,凡与本集团有关的,均属于前瞻性表述。本集团并无义务不断地更新这些预测性陈述。
这些前瞻性表述是基于本集团管理层在做出表述时对未来事务的现有看法、假设、期望、估计、预测和理解。这些表述并非对未来发展的保证,会受到风险、不确性及其他因素的影响,有些是超出本集团的控制范围,难以预计。因此,受我们的业务、竞争环境、政治、经济、法律和社会情况的未来变化及发展的影响,实际结果可能会与前瞻性表述所含资料有较大差别。
本集团、本集团董事及雇员代理概不承担(1)更正或更新本网站所载前瞻性表述的任何义务;及(2)若因任何前瞻性表述不能实现或变成不正确而引致的任何责任。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。